姚珂医生的科普号
- 典型病例 一种容易误诊为肺大泡的恶性肺结节
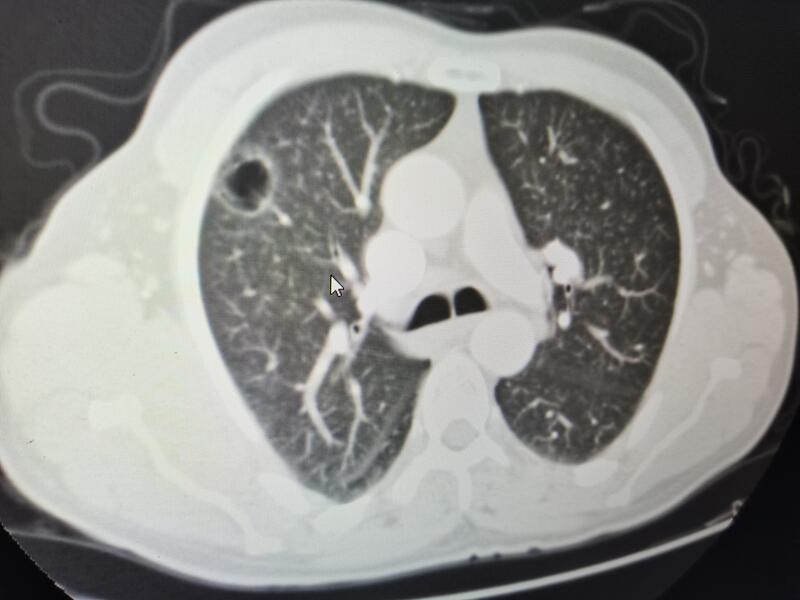
在临床工作中,常见到一种特殊的肺结节,其影像表现为空泡状,泡壁较厚,密度明显高于周围正常肺组织,边界欠清晰,厚薄不均,而被误诊为肺大泡。其实是一种早期肺癌的典型表现,需引起重视!图一、影像学诊断:右肺上叶肺大泡,术后病理诊断:右肺上叶微小浸润性腺癌。图二、影像学诊断:右肺上叶肺大泡,术后病理诊断:右肺上叶原位腺癌。这一类型的空泡型肺结节,泡壁明显增厚,厚薄不均,边界欠清晰,密度明显增高,实为细胞增生堆集,病理表现为沿肺泡壁排列聚集的肿瘤细胞,多为原位腺癌或微浸润性腺癌。若能早期明确诊断,及时治疗,预后较好。但是若误诊,定期随访,有发展为浸润性腺癌的风险,预后较差。良性肺大泡多表现为薄壁、均勻一致的线状影,中间为无肺纹理的含气空泡,与恶性空泡型肺结节的主要区别在泡壁的表现不一样,这需要引起重视!肺结节型肺癌的早诊早治是提高生存率的关键因素。
 姚珂 副主任医师 医生集团-重庆 线上诊疗科1008人已读
姚珂 副主任医师 医生集团-重庆 线上诊疗科1008人已读 - 就诊指南 如何用手机翻拍医用胶片并上传清晰影像图片
随着手机的普及和互联网医疗的不断发展,通过微信、QQ、APP医疗平台寻找医生进行远程诊疗、咨询变得越来越普遍,在这些诊疗活动中,医生不可避免的需要查看患者m影像资料,而笔者经常看到的是一些病患发来的影像资料质量太差,严重影响观看,甚至完全无法使用,不能对疾病的诊断提供帮助。 下面几张患者手机翻拍后通过网络上传来的图片,倾斜、反光、黑白不均、模糊不清,有些患者把胶片拿在手上对着灯光、直接贴在窗户上、放在桌面上拍摄等,上传的图片基本属于废图,对于医生阅片毫无意义。 怎么用手机翻拍比较清晰的医用胶片? 如何用手机翻拍自已检查的影像资料,在向医生咨询、远程会诊及讨论时上传有用的信息呢? 1、拍摄背景选择: 1)、可使用电脑显示器作为背景进行拍摄。 在电脑打开幻灯软件PowerPoint(PPT),建一个纯白色的空白文档,全屏播放模式下,即可实现全屏白色。将胶片贴于显示器上进行拍照。 2)、将白纸或白布贴于窗户玻璃上,然后将医用胶片贴于白纸或白布上拍照。 3)、如果能在医院找到医生专用的观片灯,则为最佳选择。 2、拍摄注意事项: 1)、手机拍摄时切记关闭闪光灯! 2)、拍摄者着深色衣服,避免浅色衣服在图片上形成反光影像。 3)、白天拍摄,窗户外光亮,室内关灯。 4)、拍摄时正对图片,注意横平竖直,避免歪斜。 5)、拍摄一张图片内有两张影像时,先合起来拍一张,再分开各拍一张。 6)、磁共振和CT片包含很多张小的影像图片,单纯拍一张图片,细节看不清楚,因此需要将图片进行分区并局部放大,按顺序进行拍摄并编号,尽可能将细节拍摄清楚。 7)、拍摄时,将图片的文字信息拍摄清楚,尽可能多的保留图片的所有信息。 8)、记住重要的一点:图片上下左右不能放反(看文字)。 9)、拍摄完毕,按顺序、按编号原图发送(切忌PS、美颜和美图修改)。 10)、在做磁共振、CT等检查时,可以到放射科刻录原始影像数据光盘,一般的医院都会提供,但需要另行收取工本费。
 姚珂 副主任医师 医生集团-重庆 线上诊疗科5405人已读
姚珂 副主任医师 医生集团-重庆 线上诊疗科5405人已读 - 医学科普 肺错构瘤概述
肺错构瘤是一种起源于支气管的间叶性良性肿瘤,是肺部最常见的良性肿瘤,男性多于女性,好发于中老年人,平均年龄40岁以上,发病率约为0.25%,占肺部良性肿瘤的75~77%,仅次于肺癌和肉芽肿性病变。 其病理组织成分有软骨、纤维组织、平滑肌、脂肪。依据肿瘤内组织成分不同,可分为软骨型和纤维型肺错构瘤;根据发生部位分为中央型和周围型肺错构瘤,以周围型多见。 临床上肺错构瘤可分为三型:1、肺内型最多见,原发于肺表面部位;2、腔内型亦称为支气管内型,占5~10%;3、弥漫型肿瘤数目两个以上,位于一侧肺或双侧肺,女性多见。 临床表现 大多无明显症状,常于体检时胸片发现肺部阴影,部分病人因肿瘤较大压迫或刺激支气管出现咳嗽、咳痰、胸闷不适等症状。腔内型出现症状较早,常伴有哮鸣,甚至引起严重呼吸困难和发绀,被误诊为哮喘。若肿瘤造成管腔狭窄、部分梗阻,可引起继发感染。 肺错构瘤的CT影像学特点 1、结节直径多小于2.5cm; 2、病灶边缘光滑,瘤肺交界面截然,呈圆形或卵圆形,少数病灶边缘可出现浅分叶,甚至深分叶及脐凹,但少见毛刺,尤其是细小的毛刺; 3、结节内CT值-40~140HU的局灶性脂肪组织或与脂肪区共存的CT值大于170HU的钙化区,无空洞是其典型CT表现; 4、增强后病灶无强化或轻度强化; 5、随访病灶生长缓慢但会逐渐增大,钙化逐渐增多。 治疗 肺错构瘤大多数为良性,恶性仅占0.5%左右,但文献也有恶性报道。由于本病有时难于与周围型肺癌鉴别,因此多主张早期手术。对中、老年人肺孤立性病变不能肯定为良性者,均应做手术探查。 大多数肺错构瘤病例可采用肿瘤摘除术或肺楔形切除术。若肿瘤位于肺门,体积巨大,或与肺门支气管、血管不易分离,或已造成远端肺组织不可逆病理改变时,可行肺叶切除术,很少需做全肺切除。无论是肿瘤摘除或楔形切除,术后均无复发。
姚珂 副主任医师 医生集团-重庆 线上诊疗科1815人已读 - 医学科普 肺隔离症概述
肺隔离症也称为有异常动脉供血的肺囊肿症,是临床上相对多见的先天性肺发育畸形,占肺部疾病的0.15~6.4%,为胚胎时期一部分肺组织与正常肺主体分离,单独发育并接受体循环动脉的异常动脉供血,所形成无呼吸
姚珂 副主任医师 医生集团-重庆 线上诊疗科730人已读 - 医学科普 食管裂孔疝概述
食管裂孔疝是指腹腔内脏器(主要是胃)通过膈肌食管裂孔进入胸腔所致的疾病。食管裂孔疝在膈疝中最常见,达90%以上,属于消化内科疾病。患者可无症状或症状轻微,其症状轻重与疝囊大小、食管炎症的严重程度有关。 本病可发生于任何年龄,但症状的出现随年龄的增长而增多,在有可疑症状者的常规X线钡餐检查中,食管裂孔疝的检出率为11.8%。其发病率中女性多于男性,为1.5~3:1。 病因 正常食管裂孔由左右膈肌脚在第1~4腰椎左前方包绕而成,有数层组织,如胸膜、纵隔脂肪、胸内筋膜、腹内筋膜等,将胸腔与腹腔分隔。此外,胃食管结合部(位于隔肌下方临近腹腔内)通过食管下段环形肌纤维的张力性收缩、胸腹腔之间的压力差(静息状态下该段食管腔内压力既高于颈胸段食管,又高于胃底部)作用、隔肌角的弹环夹夹闭作用等,从而保持关闭,当吞咽进食后立即松驰,保证食物按食管到胃的单向运动。其次,食管腹腔段的适宜长度、His角的活瓣作用,也起到抗反流作用,防止胃酸向食管反流。 膈食管韧带可封闭裂孔、抵抗腹压、固定食管、防止胃进入胸腔。 先天性发育异常:膈肌脚、食管裂孔周围组织发育不良。 后天因素:膈食管韧带退变、松驰;腹腔内压力升高;食管痉挛;手术和外伤。 发病机制 膈食管裂孔的扩大,环绕食管的膈肌脚薄弱等,致使腹段食管、贲门或胃底随腹压增高,经宽大的裂孔而进入纵隔,进而引起胃食管反流、食管炎等一系列病理改变。 病理分型:常用的是Barrett分型,根据食管裂孔发育缺损的程度、突入胸腔的内容物多寡、病理及临床改变,将食管裂孔疝分为3型。Ⅰ 型:食管裂孔滑动疝;ll 型:食管旁疝;ⅠⅠⅠ 型:混合型。其分型简单、实用,被国内外普遍采用。 临床表现 不同发病年龄、不同病理类型的临床表现各有其特点。疼痛是最常见的症状,还包括反流返酸、打嗝和反胃、咽下困难、吞咽障碍、上消化道出血以及心脏、肺和纵隔压迫症状。 诊断 结合上述临床特点及以下几项检查可明确食管裂孔疝的诊断:X 线食管、胃造影检查表现为食管末端、胃食管交接部、部分胃经食管裂孔疝至膈上,且随体位改变而上下移动,His角变钝,胃食管反流,食管扩张,裂孔开大。内窥镜检查可见食管粘膜水肿、充血、糜烂、溃疡、出血、狭窄等不同程度病理改变,贲门口松驰,胃粘膜疝入食管腔等。胸部CT影像学表现可见食管下段及胃等腹腔脏器经扩大的食管裂孔疝入胸腔。 治疗 治疗食管裂孔疝的目的在于防止胃食管反流,促进食管胃排空以及缓和或减少胃酸的分泌。需根据具体病情选择适当的治疗方法。 无症状者一般不需要治疗,有症状者大多数经内科治疗可以得到不同程度的缓解,仅少数患者要外科治疗。 非手术治疗:婴儿食管裂孔滑动疝、症状轻微的小型食管裂孔滑动疝在发育过程中可以自行消失或好转,可首选保守治疗。 手术治疗:手术的目的是使食管下段及食管胃结合部恢复到其腹腔内的正常位置,并加强食管下括约肌。手术主要解决的问题有:将食管腹腔段恢复到正常位置;固定食管、贲门;将变钝的His角变锐;修复、缩小扩大的食管裂孔;防止反酸。 手术适应症:有严重胃食管反流、呕吐频繁导致营养摄入不足并影响生长发育、经非手术治疗无效的先天性食管裂孔滑动疝;并发严重食管炎、溃疡、出血,或出现严重贫血经内科治疗无效者;严重食管狭窄而行食管扩张无效者;食管旁疝、混合型食管裂孔疝或疝囊巨大、反复嵌顿而产生心肺压迫症状者;反流性食管炎恶变、不能排除恶变或柱状上皮覆盖者;食管旁疝发生嵌顿,经即刻插入胃管减压不成功或症状不改善者,应急诊探查。 手术方式有经胸和经腹两种入路,各有利弊。经胸入路视野显露好,但创伤大,对心肺影响大,适用于食管裂孔开孔大,估计粘连重、胃扭转以及疝入右侧胸腔者,食管过短者需采用些入路。经腹入路侵袭小,恢复快,可同时检查腹腔内脏器,处理消化道畸形,且幽门成型和胃底折叠术操作方便。适用于低龄的食管裂孔疝患者。近年来,随着腔镜技术的飞速发展,胸腔镜和腹腔镜微创手术已逐渐取代常规开胸和剖腹手术。 手术疗效:经手术治疗的病例,绝大多数可达到症状完全缓解的目的。少数病例可有早期反流。
姚珂 副主任医师 医生集团-重庆 线上诊疗科1557人已读 - 学术前沿 最新:Ⅰ-ⅠⅠⅠB期非小细胞肺癌完全切除术后辅助治疗指南概述
肺癌是我国发病率和死亡率最高的肿瘤,其发病率和死亡率分别为57.26/10万人和45.87/10万人,是第二位恶性肿瘤的近2倍,在初诊确诊的患者中约30%为可切除的早中期NSCLC。 目前对其治疗和管理,尤其是术后分子检测、辅助治疗及随访均欠规范且存在诸多争议。在此背景下,中国抗癌协会肺癌专业委员会、中华医学会肿瘤学分会肺癌学组及中国胸部肿瘤研究协作组组织专家,在充分吸收全球最新临床研究成果,参考国际指南和中国国情,针对I-ⅠⅠⅠB期NSCLC肿瘤完全切除术后患者,对诊断、分子检测、辅助治疗及术后管理等问题进行规纳总结,以规范NSCLC患者的术后辅助治疗方法,达到降低复发率、延长生存时间和提高生活质量的目的。 指南、证据级别 1类:水平高,来源于严谨的荟萃分析、大型随机对照临床研究; 2类:水平稍低,来源于一般质量的荟萃分析、小型随机对照临床研究、设计良好的大型回顾性研究、病例-对照研究; 3类:水平低,来源于非对照的单臂临床研究、病例报告、专家观点。 推荐级别 一致推荐:投票讨论100%专家完全达成一共识; 推荐:投票讨论75%~99%专家达成共识; 存在分歧但推荐:投票讨论50%~74%专家达成共识,少数专家存在分岐; 不推荐:投票讨论<50%一致,不做推荐。 NSCLC肿瘤完全切除术后诊断及检测 一致推荐: 1、良好的手术切除标本病理诊断应包括:肿瘤部位、组织学亚型、分化程度、累及范围、切缘及必要的特殊染色、免疫组化结果或分子病理检测结果,并且其描述和结论应满足临床分期的需要,建议提供pTNM分期(采用IASLC/UICC第八版标准); 2、需要做术后辅助治疗的NSCLC患者,术后病理标本常规进行组织学诊断时,建议同步进行EGFR基因突变检测;检测范围应涵盖EGFR18、19、20、21号外显子,以包括其主要的突变类型19号外显子缺失突变(19del)、21号外显子点突变(L858R,L861Q)、18号外显子点突变(G719X)及20号外显子插入突变(20ins)和点突变(T790M,S768I)。 NSCLC肿瘤完全切除术后辅助治疗手段概述 一、辅助化疗 一致推荐:1、辅助化疗前需综合评估辅助化疗的收益和风险;2、以下患者不宜采用辅助化疗:体力状态较差(ECOG评分>2或kPS评分<60)、严重肝肾功能异常(实验室指标超过正常值2倍)、存在严重合并症、活动性感染、持续性发热、严重出血倾向、造血功能异常(血红蛋白<80g/L,中性粒细胞<1.5×109/L、血小板<100×109/L)的NSCLC患者;3、辅助化疗的方案采用以顺铂为基础的双药方案,对于无法耐受顺铂的患者,可采用卡铂为基础的双药方案;4、待患者术后体能状况基本恢复正常,可开始辅助化疗,一般在术后4~6周开始,建议最晚不超过手术后3个月;5、术后辅助化疗常规推荐4周期,更多化疗周期不会增加患者获益,反而可能增加不良反应。 二、辅助靶向治疗 一致推荐:1、EGFR-TkI(奥西替尼、埃克替尼、厄洛替尼,尤其是奥西替尼)辅助治疗可延长EGFR突变阳性早中期NSCLC患者的DFS,特别是奥西替尼可显著降低远处复发脑转移的风险,可作为ⅠI-ⅠIlA期EGFR突变阳性NSCLC患者术后标准治疗方案;2、医生根据患者术后体能状况恢复情况决定启动EGFR-TkI辅助治疗的时间,最晚不超过10周;3、对于接受过辅助化疗的EGFR突变阳性患者,可继续接受第三代EGFR-TkⅠ奥希替尼辅助治疗,开始奥西替尼辅助治疗的时间通常不晚于术后26周;4、术后EGFR-TkⅠ辅助治疗的时间应不少于2年。 三、辅助放疗 1类证据:1、对于N0和N1 NSCLC患者,不推荐行术后辅助放疗;2、对于N2 NSCLC患者肿瘤完全切除术后,不推荐行辅助放疗。 四、新辅助免疫治疗 3类证据:EGFR突变阴性的NSCLC患者,如新辅助采用免疫检查点抑制剂治疗且有效,建议MDT讨论决定辅助治疗方案。 五、EGFR突变阳性的I-ⅠⅠIB期NSCLC肿瘤完全切除术后辅助治疗详述: 1、ⅠA期:定期随访,不推荐进行辅助化疗(1类证据,推荐); 2、ⅠB期:可考虑应用奥西替尼辅助治疗(1A类证据,推荐); 3、IⅠA、llB期:推荐奥西替尼(1A类证据)或埃克替尼(1B类证据)辅助治疗(一致推荐); 4、IⅠⅠA、lⅠⅠB期:推荐奥西替尼(1A类证据)、埃克替尼(1B类证据)或厄洛替尼(2类证据)辅助治疗,且优先推荐奥西替尼辅助治疗(一致推荐)。 六、EGFR突变阴性的I-ⅠⅠⅠB期NSCLC肿瘤完全切除术后辅助治疗详述 1、ⅠA期:定期随访,不推荐进行辅助化疗(1A类证据,推荐); 2、ⅠB期:不推荐辅助化疗(1类证据),对于其中存在高危因素的患者,推荐进行多学科综合评估,结合评估意见以及患者意愿,可考虑术后辅助化疗(3类证据)。高危因素包括:低分化肿瘤(包括乳头型腺癌、神经内分泌肿瘤等,但不包括分化良好的神经内分泌肿瘤),脏层胸膜侵犯、脉管侵犯、气腔内播散等; 3、IⅠ-ⅠⅠⅠB期:推荐进行辅助化疗(1A类证据,一致推荐)。 NSCLC患者肿瘤完全切除术后随访 1、一致推荐有必要进行密切随访; 2、对于出现新发症状或症状加重的患者,推荐立即随访。
姚珂 副主任医师 医生集团-重庆 线上诊疗科3633人已读 - 医学科普 肋骨骨折的治疗策略
胸部创伤是目前创伤致死的第二大病因,肋骨骨折是最常见的损伤,约占全部创伤的10%。根据创伤部位及严重程度,肋骨骨折可以从单根到多根,而双侧严重肋骨骨折对呼吸功能影响更明显,可出现胸痛、呼吸困难、肺炎甚至呼吸功能衰竭而需要呼吸机支持,肋骨骨折的死亡率在2~20%。三根以上肋骨骨折且每根肋骨2个或以上部位骨折称之为连枷胸,连枷胸往往合并反常呼吸和严重肺挫伤,出现呼吸功能衰竭而需要呼吸机支持。肋骨骨折是严重创伤的标志,骨折数量越多死亡率越高。 肋骨骨折治疗的历史及争议 在过去的50年里,胸部创伤肋骨骨折大部分采用非手术治疗,但容易出现肺部感染、败血症等相关并发症,胸壁畸形以及慢性疼痛等症状。非手术治疗包括保持气道通畅、控制浮动胸壁、有效镇痛、限制性液体复苏、必要时采用正压呼吸机支持。连枷胸非手术治疗的患者肺炎发生率27~70%,死亡率在25~51%。随着科技和诊治手段的进步,特别是近年来开展的各种肋骨骨折内固定技术使连枷胸死亡率降低。可减少机械通气时间、降低呼吸机相关并发症、缩短住院时间。 肋骨骨折的影像学诊断 X线和CT是目前常用的肋骨骨折影像学方法,常规胸部正位X线检查,可初步判定患者的受伤情况,还可提供部分胸壁肋骨骨折的影像证据。胸部CT可以显示胸壁软组织、骨性胸壁、胸膜、肺组织及纵隔等情况。骨性胸廓CT三维成像不但可以提供清晰的骨折断端,而且能更好地显示胸廓骨性结构的完整性,为肋骨内固定提供有力的影像学支持。肋骨、肋软骨曲面断层CT成像可清晰显示X线或胸廓三维成像不能明确诊断的助骨、肋软骨骨折或单面骨皮质骨折,对肋骨、肋软骨骨折的定性诊断起到决定性作用,对骨折的愈合程度包括骨不连都有很好的诊断价值。 肋骨骨折内固定手术治疗的价值 目前多数研究对连枷胸肋骨内固定的价值达成共识:手术治疗可以消除胸壁反常呼吸运动,改善患者呼吸情况,减少呼吸机通气支持时间,从而减少肺部感染、败血症等呼吸机相关并发症,恢复胸壁稳定性,消除胸壁畸形、降低肋骨骨折不愈合或畸形愈合、慢性疼痛的症状,减少ICU治疗时间,减轻患者经济负担,尽快恢复正常生活和工作状态。 肋骨内固定手术指征 肋骨骨折的手术征:1、呼吸机依赖、有明显反常呼吸的连枷胸患者,没有严重的肺挫伤及颅脑外伤;2、肋骨骨折断端运动导致或加剧患者疼痛,镇痛治疗失败;3、胸壁塌陷、软化导致胸壁疝,肋骨骨折断端错位明显,限制肺复张或刺入肺脏;4、症状明显的肋骨骨折不连;5、开胸手术的其它指征。 肋骨骨折内固定常用的内固定物 肽合金锁定板:肋骨前置板皮质螺钉固定是一个标准的,经得起比较和时间考验的技术。动力加压接骨板和锁定螺钉设计是较新的没计创新,能稳定固定正常和骨质疏松的肋骨。 髓内固定装置:稳定性有待加强,适合应用于难以完全暴露的部位,如肩胛骨后方的肋骨骨折。克氏针的应用已逐渐减少。 Judet夹:是一种可弯曲塑形的,通过两侧边卷曲爪形结构,在骨折断端两侧环抱固定肋骨上、下缘的肽合金内固定物,可以桥接两个肋骨骨折断端。 镍钛记忆合金肋骨环抱器:是近年来应用于临床的一种内固定设备。是一种形状记忆合金,它能将自身的塑形在某一特定温度下自动恢复为原始形状。应用冰冻无菌盐水使环抱器处于可塑形状态,塑形完成后迅速固定到肋骨骨折断端,在人体体温下形态迅速恢复,从而牢固固定肋骨。 可吸收内固定装置:可吸收肋骨钉或肋骨板是由聚乳酸聚合物设计制成,已被成功应用于创伤性连枷胸及非创伤性开胸手术。这种材质的内固定物18~24个月后在体内转化为二氧化碳和水,不用二次手术取出。 手术时机 根据损害控制外科(DCS)理论,每个创伤患者的损伤部位和严重程度不同,手术时机应依据每个受伤患者的具体情况决定,即个体化治疗。目的在于恢复机体正常的生理状态、纠正低氧、凝血功能紊乱、体温过低、酸中毒等。 多学科协作,遵从快速康复外科理念在治疗在胸部创伤及多发肋骨骨折中至关重要,是今后发展的方向。
姚珂 副主任医师 医生集团-重庆 线上诊疗科1524人已读 - 学术前沿 非小细胞肺癌新辅助免疫治疗专家共识
2021年1月10日 共识1: IB-IⅠⅠA期的可切除NSCLC患者可考虑应用术前新辅助免疫治疗或联合含铂药物化疗。 共识2: 暂无证据支持分子标志物能够预测免疫治疗的疗效,因此,新辅助免疫治疗的应用无需监测标志物;但是存在EGFR敏感突变及ALK融合等潜在的负性预测因子的患者,应谨慎选择新辅助免疫单药治疗。 共识3: 推荐2~4周期的新辅助免疫治疗,每2周期应进行疗效评价,修正治疗方案。 共识4: 推荐优先应用PET/CT进行疗效评价,可联合血清标志物或ctDNA负荷。 共识5: 手术应在末次新辅助治疗后4~6周进行。 共识6: 没有证据支持新辅助免疫治疗影响手术的安全性与实施。 共识7: 新辅助免疫治疗后应由专业的病理医生评估、报告病理学缓解情况,包括主要病理学缓解和完全病理学缓解。 共识8: 接受新辅助免疫治疗未进展的患者,在手术后应重启免疫治疗且可维持治疗1年。 共识9: 临界可切除的局部晚期NSCLC患者可以应用免疫治疗或诱导化疗,再分期后重新评估手术可能性。
姚珂 副主任医师 医生集团-重庆 线上诊疗科2645人已读 - 医学科普 食管平滑肌瘤诊治进展
食管平滑肌瘤是最常见的食管良性肿瘤,随着其体积的不断增大,可导致如吞咽困难等临床表现,严重影响患者生活质量。 食管平滑肌瘤的发病特点 食管平滑肌瘤占所有食管良性病变的70%~80%,好发于20~50岁男性,通常位于食管的下2/3段。绝大多数起源于食管肌层,极少数起源于粘膜肌层。肿瘤以单发多见,可呈类圆形、马蹄形、哑铃形及螺旋形盘绕等不规则形。肿瘤位于壁内者97.9%,管壁外生长者1.4%,呈息肉状生长者0.7%,有5%的患者肿瘤完全包绕食管。食管平滑肌瘤大小不一,目前报道最大者长径达20cm,最小为0.5cm x 0.5cm x 0.5cm。若肿瘤直径<5cm,绝大多数无症状,当肿瘤长到足够大时可出现相关临床症状,常见症状有吞咽困难、烧心和胸骨后疼痛。 食管平滑肌瘤的诊断 1、食管造影:主要表现为食管腔内的充盈缺损,病变与食管壁成锐角,局部粘膜呈“涂沫征”、“环形征”,粘膜无破坏,管壁易扩张。 2、CT:能更好地显示食管与周围结构的关系,对区别食管本身的疾病和周围病变的外压性改变有较大价值。主要表现为局部均质的软组织肿块,并显示瘤体外形及大小。 3、电子内镜及超声内镜:电子内镜更直观,对病变部位、大小、形态以及表面情况描述更具体。内镜下典型表现为食管粘膜有突出的病变,粘膜表面光整。超声内镜对病变的描述尤其是病变来源的确定更精准,不仅能发现局限于食管壁的病变,还能准确评估病变的性质、大小和部位,以及其与周围器官的关系,并根据这些特征来决定最佳治疗方式。超声内镜下肿瘤表现为形态规则、均匀低回声肿物,且被完整清晰的包膜所包绕。是目前临床诊断食管平滑肌瘤的金标准。 食管平滑肌瘤的治疗 对无症状平滑肌瘤患者的治疗方式目前仍存在争议。一些学者建议对病变<5cm的病例应只进行观察和随访;而另一些学者则认为病变切除适用于病变介于1㎝~5cm的患者,是因为有罕见的癌变可能,也为了明确组织病理学诊断。而对于<1cm的病变不应行手术治疗,建议每年或每2年行内镜或影像学检查随访。 传统手术治疗:开胸或开腹肿瘤摘除术曾被认为是食管平滑肌瘤最适宜的手术方式。适用于:(1)胸腔广泛粘连或不能耐受单侧肺通气;(2)大型食管平滑肌瘤或肿瘤剔除困难;(3)术中冰冻病理提示恶性。绝大多数患者只需行肿瘤切除术,仅极少数患者需要选择食管切除术和食管-胃吻合术,其手术指征包括肿瘤巨大切除难度大(甚至大于常规的限制8cm),或伴有食管壁广泛损伤,以及术后形成食管瘘的风险较高。 内镜技术和微创技术治疗:电子内镜下切除方式包括内镜粘膜下剥离术(ESD),内镜粘膜下挖除术(ESE)和内镜下全层切除(EFR),经内镜粘膜下隧道肿瘤切除术(STER)是近年来飞速发展的一项新型内镜技术,对摘除起源于肌层的食管平滑肌瘤是安全有效的,但对于直径>35cm的病变该方法仍存在技术挑战。微创胸腔镜或腹腔镜手术以一具带来的更短的术后住院时间、更好的肺复张及更少的肺部并发症、较轻微的伤口疼痛和术后不适感、良好的外观等优势逐渐取代传统手术称为食管平滑肌瘤的标准治疗方法。 无论采取哪种手术方式,手术的关注重点是完全剔除肿瘤、避免食管粘膜损伤及保留食管的迷走神经和血供。
姚珂 副主任医师 医生集团-重庆 线上诊疗科1450人已读 - 医学科普 肺癌免疫治疗药物汇总
化疗已经不再是肺癌患者的唯一选择,如果经基因检测之后有用药靶点,靶向药物已经成为了肺癌患者的新选择,可是如果没有靶向基因突变、或者患者已经对化疗、靶向治疗产生耐药、肿瘤不再能被控制,那么免疫治疗就成了新的希望。 免疫治疗常用的生物标志物中PD-L1是被广泛认可的“不完美”标志物,当前批准应用于非小细胞肺癌的免疫治疗方案中,多个一线治疗方案都要求必须检测PD-L1表达状态。对于PD-L1阳性(≥1%~49%)且没有靶向基因突变的肺癌(非鳞NSCLC)患者,UNCC指南推荐化疗联合免疫药物治疗,然而,在PD-L1检测结果呈阴性的患者中,51%的患者使用联合免疫药物的方案是有效的,所以,如果我们只以PD-L1检测结果作为唯一标准的话,有相当一部分患者可能错失了免疫治疗机会。其它常用的免疫治疗生物标志物还有TMB(肿瘤基因突变负荷)、m IHC(肿瘤免疫微环境检测)、GEP(基因表达谱)等。 目前国内外常用肺癌免疫治疗药物有: 进口 PD-1:帕博利珠单抗(k 药)、纳武利尤单 抗(O 药) CTLA-4:伊匹单抗(Y药,与 O 药联用) PD-L1:阿替利珠单抗(T 药)、度伐利尤 单抗(I药) 国产(PD-1) 卡瑞丽珠单抗、替雷利珠单抗、信迪利单抗、特瑞普利单抗 帕博利珠单抗 (Pembrolizumab,可瑞达,Keytruda/K药) 适应症: NSCLC:1)单药用于一线治疗PD-L1阳性的、EGFR/ALK阴性的局部晚期或转移性非小细胞肺癌;2)联合培美曲塞和铂类化疗药物,用于一线治疗EGFR/ALK阴性的转移性非鳞状非小细胞肺癌;3)联合卡铂和紫杉醇/白蛋白紫杉醇,用于一线治疗转移性鳞状非小细胞肺癌;4)用于铂类化疗进展后的PD-L1阳性NSCLC。 SCLC:用于既往接受过铂类为基础的化疗和至少一种其它治疗后发生疾病进展的小细胞肺癌。 药品规格:100mg/4ml。 用法用量:a、200mg Q3w 或 400mg Q6w;b、国内说明书为: 2 mg/kg Q3w,静脉输注30分钟以上,直至出现疾病进展或不可接受的毒性。 不良反应:疲劳、瘙痒、皮疹、腹泻和恶心。 纳武利尤单抗 (Nivolumab,欧狄沃,Opdivo/O药) 适应症: NSCLC:1)纳武利尤单抗联合伊匹单抗的双免疫组合一线治疗驱动基因阴性的PD-L1>1%的晚期非小细胞肺癌;2)纳武利尤单抗+伊匹单抗联合2周期化疗一线治疗驱动基因阴性的晚期非小细胞肺癌;3)单药用于治疗EGFR/ALK阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌。 SCLC:2020年12月31日,O药撤回在美获批的小细胞肺癌适应症。 药品规格:40mg/4ml,100mg/10ml,240mg/24ml。 用法用量:a、O药 3mg/kg Q2w + 伊匹单抗1mg/kg Q6w;b、O药 3mg/kg Q2w + 伊匹单抗1mg/kg Q6w + 2周期含铂类的双药化疗;c、240mg q2w或 480mg q4w;d、国内说明书为:3mg/kg或240mg固定剂量,静脉滴注每2周一次,直至出现疾病进展或产生不可耐受的毒性。在30分钟或60分钟时间静脉输注本品。 不良反应:疲劳、瘙痒、皮疹、腹泻和恶心。特别注意免疫相关不良反应性肺炎、肝炎、肾炎、结肠炎、内分泌疾病等。 伊匹单抗 (Ipilimumab,易普利姆玛,Yervoy/Y药) 适应症:1)与nivolumab(纳武利尤单抗)联合,用于一线治疗PD-L1阳性,EGFR/ALK阴性的转移性非小细胞肺癌(NSCLC)成年患者;2)联合铂类化疗,用于EGFR/ALK阴性的转移性/复发性非小细胞肺癌(NSCLC)成年患者。 药品规格:50mg/10ml,200mg/40ml 用法用量:30mg/kg,90分钟内静脉滴注完毕,每3周一次,连续使用4个周期。 不良反应:联合纳武利尤单抗副作用为乏力、皮疹、瘙痒、腹泻、肌肉骨骼疼痛、咳嗽、发热、食欲减退、恶心、腹痛、关节痛、头痛、呕吐、呼吸困难、头晕、甲状腺功能减退和体重减轻。联合纳武利单抗以及化疗常见副作用为疲劳、肌肉骨骼疼痛、恶心、腹泻、皮疹、食欲减退、便秘和瘙痒。 阿替利珠单抗 (Atezolizumab,泰圣奇,Tecentriq/T药) 适应症: NSCLC:1)一线治疗EGFR/ALK阴性,PD-L1高表达(TC≥50%或IC≥10%)的转移性NSCLC患者;2)“阿替利珠单抗 + 卡铂 + 白蛋白紫杉醇”用于无EGFR/ALK突变的非鳞状NSCLC患者的一线治疗;3)“阿替利珠单抗 + 卡铂 + 紫杉醇”用于无EGFR/ALK突变的非鳞状NSCLC患者的一线治疗;4)用于铂类化疗后进展的NSCLC。 SCLC:与卡铂和依托泊苷联合用于广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。 药品规格:840mg/14ml,1200mg/20ml 用法用量: NSCLC:1)单药,840mg q2w 或1200mg q3w 或1680mg q4w;2)联合化疗/或抗血管治疗,1200mg q3w,在化疗和抗血管治疗前使用;完成4~6周期化疗后,继续T药840mg q3w或1680mg q4w,直至出现疾病进展或产生不可耐受的毒性。 SCLC:在诱导期,第1天静脉输注阿替利珠单抗,推荐剂量为1200mg,继之以静脉输注卡铂,之后是依托泊苷,第2天和第3天静脉输注依托泊苷。该方案每3周给药一次,共4个治疗周期。诱导期之后是无化疗的维持期,在此期间每3周静脉输注一次1200mg阿替利珠单抗,直至出现疾病进展或产生不可接受的毒性。输注时间大于60分钟。 不良反应:疲乏、食欲下降、恶心、咳嗽、呼吸困难、发热、腹泻等。特别注意免疫相关性肺炎。 度伐利尤单抗 (Durvalumab,英飞凡,IMFINZI/I药) 适应症: NSCLC:适用于在接受铂类药物为基础的化疗同步放疗后出现疾病进展的不可切除、III期非小细胞肺癌(NSCLC)患者的治疗。 SCLC:与卡铂/顺铂和依托泊苷联合用于广泛期小细胞肺癌患者的一线治疗。 药品规格:500mg/10ml,120mg/2.4ml 用法用量:a、lll期NSCLC:≥30kg,10mg/kg q2w;b、SCLC:≥ 30kg,1500mg/kg q3w 联合化疗,后续单药维持10mg q2w。输液时间大于60分钟。 不良反应:咳嗽、乏力、肺炎、上呼吸道感染、呼吸困难和皮疹,恶心、乏力、特别注意免疫性肺炎、肝炎、肾炎、结肠炎等。 卡瑞丽珠单抗 (Camrelizumab ,艾瑞卡,国产) 适应症:联合培美曲塞和卡铂适用于EGFR/ALK阴性的、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗。 药品规格:200mg/瓶 用法用量:200mg/次,静脉注射每3周一次,直至疾病进展或出现不可耐受的毒性。卡瑞丽珠单抗联合化疗给药时,应首先给予卡瑞丽珠单抗静脉滴注,间隔至少30分钟后再给予化疗。 不良反应:毛细血管增生症(77.6%)、恶心、乏力、食欲下降、便秘、呕吐、水肿、皮疹、瘙痒、甲状腺功能减退等,特别注意免疫相关性肺炎、肝炎、结肠炎、内分泌疾病等。 替雷利珠单抗 (Tislelizumab,百泽安,国产) 适应症:联合紫杉醇和卡铂用于局部晚期或转移性鳞状非小细胞肺癌(NSCLC)的一线治疗。 药品规格:100mg/10 ml 用法用量:推荐剂量200mg,每3周给药一次。用药直至进展或出现不可耐受的毒性。第一次输注时间不短于60分钟,如果耐受良好,则后续每一次输注时间不短于30分钟。 不良反应:疲乏、皮疹、甲状腺功能溅退、转氨酶升高,特别注意免疫相关性不良反应如免疫性肺炎、肝炎、肾炎、结肠炎、内分泌疾病等。 信迪利单抗 (Sintilimab,达伯舒,国产) 适应症:联合培美曲塞和铂类化疗用于非鳞状非小细胞肺癌(N SCLC)的一线治疗。 药品规格:100mg/10 ml 用法用量:推荐剂量为200mg,每3周给药一次。用药直至疾病进展或出现不可耐受的毒性。 不良反应:贫血、发热、转氨酶升高、乏力、白细胞计数降低。特别注意免疫相关不良反应如免疫性肺炎、肝炎、肾炎、结肠炎、内分泌疾病等。 特瑞利珠单抗 (Tislelizumab,拓益,国产) 适应症:肺癌适应症暂未获批。 药品规格:200mg/瓶 用法用量:3mg/kg,静脉滴注每2周一次,直至疾病进展或出现不可耐受的毒性。第一次输注时间不短于60分钟,如果耐受良好,后续每一次输注时间可在30分钟完成。 不良反应:疲乏、皮疹、甲状腺功能减退、转氨酶升高。特别注意免疫相关不良反应如免疫性肺炎、肝炎、肾炎、结肠炎、内分泌疾病等。
姚珂 副主任医师 医生集团-重庆 线上诊疗科9766人已读





